
|
Меню
|
 |
|
|
|
|
|
|

|
Реферат: Белки: история исследования, химсостав, свойства, биологические функции
|
 |
|
| /td> |
Денатурированная молекула белка. Черточки обозначают связи в молекуле нативного белка, разрывающиеся при денатурации |
|
Необратимое осаждение связано с глубокими внутримолекулярными изменениями
структуры белка, что приводит в потере ими нативных свойств (растворимости,
биологической активности и др.). Такой белок называется денатурированным, а
процесс денатурацией. Денатурация белков происходит в желудке, где
имеется сильнокислая среда (рН 0,5 – 1,5), и это способствует расщеплению
белков протеолитическими ферментами. Денатурация белков положена в основу
лечения отравления тяжелыми металлами, когда больному вводят per os (“через
рот”) молоко или сырые яйца с тем, чтобы металлы денатурируя белки молока или
яиц. Адсорбировались на их поверхности и не действовали на белки слизистой
оболочки желудка и кишечника, а также не всасывались
в кровь.
Размер белковых молекул лежит в пределах 1 мкм до 1 нм и, следовательно, они
являются коллоидными частицами, которые в воде образуют коллоидные
растворы. Эти растворы характеризуются высокой вязкостью, способностью
рассеивать лучи видимого света, не проходят сквозь полупроницаемые мембраны.
Вязкость раствора зависит от молекулярной массы и концентрации растворенного
вещества. Чем выше молекулярная масса, тем раствор более вязкий. Белки как
высокомолекулярные соединения образуют вязкие растворы. Например, раствор
яичного белка в воде.
 Коллоидные частицы не проходят через полупроницаемые мембраны (целлофан,
коллоидную пленку), так как их поры меньше коллоидных частиц. Непроницаемыми
для белка являются все биологические мембраны. Это свойство белковых
растворов широко используется в медицине и химии для очистки белковых
препаратов от посторонних примесей. Такой процесс разделения называется
диализом. Явление диализа лежит в основе действия аппарата “искусственная
почка”, который широко используется в медицине для лечения острой почечной
недостаточности.
Диализ (белые крупные кружки – молекулы белка, черные – молекулы хлористого
натрия)
Глава 6. Классификация белков
Все белки в зависимости от строения делятся на простые – протеины,
состоящие только из аминокислот, и сложные - протеиды, имеющих
небелковую протеистическую группу.
Коллоидные частицы не проходят через полупроницаемые мембраны (целлофан,
коллоидную пленку), так как их поры меньше коллоидных частиц. Непроницаемыми
для белка являются все биологические мембраны. Это свойство белковых
растворов широко используется в медицине и химии для очистки белковых
препаратов от посторонних примесей. Такой процесс разделения называется
диализом. Явление диализа лежит в основе действия аппарата “искусственная
почка”, который широко используется в медицине для лечения острой почечной
недостаточности.
Диализ (белые крупные кружки – молекулы белка, черные – молекулы хлористого
натрия)
Глава 6. Классификация белков
Все белки в зависимости от строения делятся на простые – протеины,
состоящие только из аминокислот, и сложные - протеиды, имеющих
небелковую протеистическую группу.
6.1. Протеины
Протеины представляют собой простые белки, состоящие только из белковой
части. Они широко распространены в животном и растительном мире. К ним
относятся альбумины и глобулины, встречающиеся практически во всех животных и
растительных клетках, биологических жидкостях и выполняющих важные
биологические функции. Альбумины участвуют в поддержании осмотического
давления крови (создают онкотическое давление), транспортируют с кровью
различные вещества. Глобулины входят в состав ферментов, составляющих основу
иммуноглобулинов, выполняющих функции антител. В сыворотке крови между этими
двумя компонентами существует постоянное соотношение – альбумино-глобулиновый
коэффициент (А/Г), равный 1,7 – 2,3 и имеющий важное диагностическое
значение.
Другими представителями протеинов являются протамины и гистоны – белки
основного характера, содержащие много лизина и аргинина. Эти белки входят в
состав нуклеопротеидов. Другой основной белок – коллаген – образует
внеклеточное вещество соединительной ткани и находится в коже, хрящах и др.
тканях.
6.2. Протеиды
Протеиды являются сложными белками, состоящими из белковой и небелковой
частей. Название протеида определяется названием его простетической группы).
Так, нуклеиновые кислоты являются небелковой частью нуклеопротеидов,
фосфорная к-та входит в состав фосфопротеидов, углеводы – гликопротеидов, а
липиды – липопротеидов.
Нуклеопротеиды. Имеют важное значение, т.к. их небелковая часть
представлена ДНК и РНК. Простетическая группа представлена в основном гистонами
и протаминами. Такие комплексы ДНК с гистонами обнаружены в сперматозоидах, а с
гистонами – в соматических клетках, где молекула ДНК “намотана” вокруг молекул
гистонов. Нуклепротеидами по своей природе являются вне клетки вирусы – это
комплексы вирусной нуклеиновой к-ты и белковой оболочки – капсида.
Хромопротеиды. Являются сложными белками, простетическая группа которых
представлена окрашенными соединениями. К хромопротеидам относятся гемоглобин,
миоглобин (бело мышц), ряд ферментов (каталаза, пероксидаза, цитохромы), а
также хлорофилл.
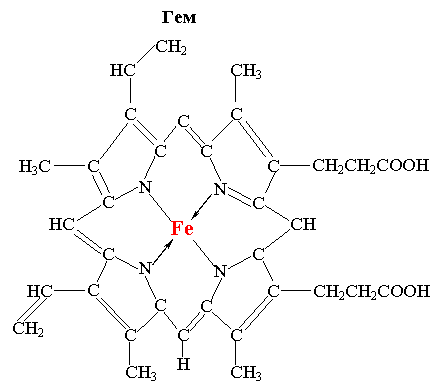
Гемоглобин (Hb) состоит из белка глобина и небелковой части
гема, включающего атом Fe(II), соединенный с протопорфирином. Молекула
гемоглобина состоит из 4-х субъединиц: двух a и двух b и соответственно
содержит четыре полипептидные цепочки двух сортов. Каждая a-цепочка содержит
141, а b-цепочка – 146 аминокислотных остатков.
Атом железа может образовать шесть координационных связей. Четыре связи
направлены к атомам азота пиррольных колец, оставшееся две связи –
перпендикулярно к плоскости порфиринового кольца по обе его стороны. Гемы
расположены вблизи поверхности белковой глобулы в специальных карманах,
образованных складками полипептидных цепочек глобина. Гемоглобин при
нормальном функционировании может находиться в одной из трех форм:
феррогемоглобин (обычно называемый дезоксигемоглобином или просто
гемоглобином), оксигемоглобин и ферригемоглобин (метгемоглобин). В
ферригемоглобине железо находится в закисной форме Fe(II), одна из двух
связей, перпендикулярных к плоскости порфиринового кольца, направлена к атому
азота гистидинового остатка, называемого проксимальным (соседним), по другую
сторону порфиринового кольца и на большем расстоянии от него находится другой
гистидиновый остаток – дистальный гистидин, не связанный непосредственно с
атомом железа. Взаимодействие молекулярного кислорода со свободным гемом
приводит к необратимому окислению атома железа гема [Fe(II) Þ Fe(III);
гем Þ гемин]. Поэтому в дезоксигемоглобине глобин предохраняет железо
от окисления.
| |
CH2 CH2
| |
           H2C CH H2C CH
O
C C
H2C CH H2C CH
O
C C
      N Fe N+
¾ Fe ¾ O
N Fe N+
¾ Fe ¾ O
 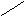
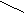 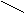 H CH H CH H CH H CH
| Плоскость порфиринового кольца |
|
| Плоскость порфиринового кольца |
|
 При взаимодействии молекулярного кислорода с гемоглобином существует небольшая,
но конечная вероятность окисления последнего: молекула O2 не
присоединяется, но окислит железо: Fe2+ + O2 Þ Fe
3+ + O2–. Поэтому при дыхании в эритроцитах
непрерывно образуется метгемоглобин. Для его восстановления в эритроците
существует специальная ферментативная система, восстанавливающая метгемоглобин
и превращающая его в нормальный дезоксигемоглобин. При нарушении этой системы
возникает тяжелое заболевание – метгемоглобинемия, при которой гемоглобин
перестает быть переносчиком кислорода.
Присоединение кислорода меняет кислотно-основные свойства гемоглобина.
Оксигемоглоин является более сильной кислотой, чем дезоксигемоглобин. Поэтому в
тканях, где значительная часть гемоглобина теряет кислород и становится более
сильным основанием, гемоглобин связывает образующуюся в ходе метаболических
внутриклеточных процессов углекислоту. В альвеолах легких дезоксигемоглобин
снова превращается в оксигемоглобин, становится более сильной кислотой и
способствует отщеплению CO2. Углекислота, освобождаемая тканями,
недостаточно хорошо растворима для эффективного переноса. С помощью фермента
карбоангидразы, ускоряющего прямую и обратную реакцию:
CO2 + H2O Û HCO3 – + H+,
Двуокись углерода превращается в хорошо растворимый бикарбонат-анион. В
капиллярах тканей отщепление кислорода повышает содержание дезоксигемоглобина,
связывающего протоны и смещающего равновесие реакции вправо. Легко растворимый
ион бикарбоната переносится кровью. В альвеолах легких гемоглобин
оксигенируется, протоны освобождаются и равновесие смещается влево. Образуется
плохо растворимая двуокись углерода CO2, которая удаляется из водной
фазы и выдыхается. Таким образом, гемоглобин работает как буфер с переменным
значением pH. Функция гемоглобина как переносчика углекислоты не менее важна,
чем его функция переноса кислорода.
Миоглобин. Хромопротеид, содержащийся в мышцах. Он состоит только из
одной цепи, аналогичной субъединице гемоглобина. Миоглобин является дыхательным
пигментом мышечной ткани. Он значительно легче гемоглобина связывается с
кислородом, но труднее отдает его. Миоглобин создает запасы кислорода в мышцах,
где его количество может достичь 14% всего кислорода организма. Это имеет
важное значение, особенно для работы мышц сердца. Высокое содержание миоглобина
обнаружено у морских млекопитающих (тюленя, моржа), что позволяет им длительное
время находиться под водой.
Гликопротеиды. Представляют собой сложные белки простетическая группа
которых образована производными углеводов (аминосахарами, гексуроновыми
кислотами). Гликопротеиды входят в состав клеточных мембран. Так, легочные
стенки бактерий построены из пептидогликанов, являющихся производными
линейных полисахаридов, несущих ковалентно связанные с ними пептидные
фрагменты. Эти фрагменты осуществляют сшивание полисахаридных цепей с
образованием механически прочной сетчатой структуры. Например, клеточная стенка
E.coli построена из полисахаридных цепей, образованных остатками
N-ацетилглюкозамина, связанными b-(1®4)связями, причем каждый второй остаток
несет присоединенный к нему по атому С3 фрагмент, образованный связанными
амидными связями остатками молочной кислоты, L-аланина, D-глутамата (через
g-карбоксил), мезодиаминонимелината и D-аланина:
При взаимодействии молекулярного кислорода с гемоглобином существует небольшая,
но конечная вероятность окисления последнего: молекула O2 не
присоединяется, но окислит железо: Fe2+ + O2 Þ Fe
3+ + O2–. Поэтому при дыхании в эритроцитах
непрерывно образуется метгемоглобин. Для его восстановления в эритроците
существует специальная ферментативная система, восстанавливающая метгемоглобин
и превращающая его в нормальный дезоксигемоглобин. При нарушении этой системы
возникает тяжелое заболевание – метгемоглобинемия, при которой гемоглобин
перестает быть переносчиком кислорода.
Присоединение кислорода меняет кислотно-основные свойства гемоглобина.
Оксигемоглоин является более сильной кислотой, чем дезоксигемоглобин. Поэтому в
тканях, где значительная часть гемоглобина теряет кислород и становится более
сильным основанием, гемоглобин связывает образующуюся в ходе метаболических
внутриклеточных процессов углекислоту. В альвеолах легких дезоксигемоглобин
снова превращается в оксигемоглобин, становится более сильной кислотой и
способствует отщеплению CO2. Углекислота, освобождаемая тканями,
недостаточно хорошо растворима для эффективного переноса. С помощью фермента
карбоангидразы, ускоряющего прямую и обратную реакцию:
CO2 + H2O Û HCO3 – + H+,
Двуокись углерода превращается в хорошо растворимый бикарбонат-анион. В
капиллярах тканей отщепление кислорода повышает содержание дезоксигемоглобина,
связывающего протоны и смещающего равновесие реакции вправо. Легко растворимый
ион бикарбоната переносится кровью. В альвеолах легких гемоглобин
оксигенируется, протоны освобождаются и равновесие смещается влево. Образуется
плохо растворимая двуокись углерода CO2, которая удаляется из водной
фазы и выдыхается. Таким образом, гемоглобин работает как буфер с переменным
значением pH. Функция гемоглобина как переносчика углекислоты не менее важна,
чем его функция переноса кислорода.
Миоглобин. Хромопротеид, содержащийся в мышцах. Он состоит только из
одной цепи, аналогичной субъединице гемоглобина. Миоглобин является дыхательным
пигментом мышечной ткани. Он значительно легче гемоглобина связывается с
кислородом, но труднее отдает его. Миоглобин создает запасы кислорода в мышцах,
где его количество может достичь 14% всего кислорода организма. Это имеет
важное значение, особенно для работы мышц сердца. Высокое содержание миоглобина
обнаружено у морских млекопитающих (тюленя, моржа), что позволяет им длительное
время находиться под водой.
Гликопротеиды. Представляют собой сложные белки простетическая группа
которых образована производными углеводов (аминосахарами, гексуроновыми
кислотами). Гликопротеиды входят в состав клеточных мембран. Так, легочные
стенки бактерий построены из пептидогликанов, являющихся производными
линейных полисахаридов, несущих ковалентно связанные с ними пептидные
фрагменты. Эти фрагменты осуществляют сшивание полисахаридных цепей с
образованием механически прочной сетчатой структуры. Например, клеточная стенка
E.coli построена из полисахаридных цепей, образованных остатками
N-ацетилглюкозамина, связанными b-(1®4)связями, причем каждый второй остаток
несет присоединенный к нему по атому С3 фрагмент, образованный связанными
амидными связями остатками молочной кислоты, L-аланина, D-глутамата (через
g-карбоксил), мезодиаминонимелината и D-аланина:
Страницы: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11
|
